Comportement des gaz
Il existe 3 gaz composant l’atmosphère terrestre : le dioxygène (O2), le dioxyde de carbone (CO2) et le diazote (N2).
On a vu que le dioxygène est nécessaire au fonctionnement de l’organisme humain. Ce gaz incolore compose plus de 20% de l'atmosphère terrestre. Le second, le CO2 , est plus souvent connu pour son rôle néfaste dans l'effet de serre. Il compose seulement 0,04 % de l'atmosphère terrestre mais, en grande quantité, devient extrêmement nocif. Enfin, le diazote (N2 d’après le vocabulaire anglais « Nitrogen ») compose plus de 78% de l’atmosphère terrestre. Il ne joue aucun rôle majeur dans la respiration humaine à la pression atmosphérique mais sa quantité est non négligeable. Nous étudierons comment leurs rôles sont modifiés vis-à-vis de la circulation sanguine en fonction de la pression ambiante, celle qui régnera à une certaine profondeur de plongée.
Tout d’abord, il faut savoir que le gaz présent à l’intérieur de la bouteille de plongée n’est pas immédiatement soumis à la pression subie par la paroi de cette bouteille. En effet, celle-ci est étudiée afin que sa forme puisse résister à la pression par l’utilisation d’une géométrie cylindrique exempte de soudures, points faibles d’une structure. Toutefois, l’air contenu à l’intérieur de ce réservoir est parfois comprimé jusqu'à 300 bar pour garantir une plus grande autonomie au plongeur.
Évidemment, un humain ne pourrait inspirer un gaz à une telle pression. Même compensée par la pression environnante, ses poumons seraient distendus par le différentiel de pression. Il existe donc un mécanisme, le détendeur qui permet de régler la pression du gaz qui passe de l’intérieur de la bouteille aux poumons du plongeur grâce à un système complexe de ressorts. Ce dernier inspirera donc un gaz à une pression absolue égale à celle imprimée par le milieu subaquatique. Toutefois, ces changements de pression influent sur le comportement des gaz.
A) Notion de pression partielle
Une première notion devant être acquise avant l’analyse du comportement de mélange gazeux (ici, l’air) est la notion de pression partielle (Pp). Celle-ci correspond à la pression qu’exercerait seul un gaz s’il occupait la totalité du volume offert au mélange, et est donnée par la loi de Dalton :
On a vu que le dioxygène est nécessaire au fonctionnement de l’organisme humain. Ce gaz incolore compose plus de 20% de l'atmosphère terrestre. Le second, le CO2 , est plus souvent connu pour son rôle néfaste dans l'effet de serre. Il compose seulement 0,04 % de l'atmosphère terrestre mais, en grande quantité, devient extrêmement nocif. Enfin, le diazote (N2 d’après le vocabulaire anglais « Nitrogen ») compose plus de 78% de l’atmosphère terrestre. Il ne joue aucun rôle majeur dans la respiration humaine à la pression atmosphérique mais sa quantité est non négligeable. Nous étudierons comment leurs rôles sont modifiés vis-à-vis de la circulation sanguine en fonction de la pression ambiante, celle qui régnera à une certaine profondeur de plongée.
Tout d’abord, il faut savoir que le gaz présent à l’intérieur de la bouteille de plongée n’est pas immédiatement soumis à la pression subie par la paroi de cette bouteille. En effet, celle-ci est étudiée afin que sa forme puisse résister à la pression par l’utilisation d’une géométrie cylindrique exempte de soudures, points faibles d’une structure. Toutefois, l’air contenu à l’intérieur de ce réservoir est parfois comprimé jusqu'à 300 bar pour garantir une plus grande autonomie au plongeur.
Évidemment, un humain ne pourrait inspirer un gaz à une telle pression. Même compensée par la pression environnante, ses poumons seraient distendus par le différentiel de pression. Il existe donc un mécanisme, le détendeur qui permet de régler la pression du gaz qui passe de l’intérieur de la bouteille aux poumons du plongeur grâce à un système complexe de ressorts. Ce dernier inspirera donc un gaz à une pression absolue égale à celle imprimée par le milieu subaquatique. Toutefois, ces changements de pression influent sur le comportement des gaz.
A) Notion de pression partielle
Une première notion devant être acquise avant l’analyse du comportement de mélange gazeux (ici, l’air) est la notion de pression partielle (Pp). Celle-ci correspond à la pression qu’exercerait seul un gaz s’il occupait la totalité du volume offert au mélange, et est donnée par la loi de Dalton :
Pp = % Gaz x Pabsolue
Exemple : calcul de la pression partielle du dioxygène à la pression atmosphérique : % O2 = 20 %, Pabs = 1 bar Donc : PpO2 = 1 x 0,2 = 0,2 bar La pression partielle du dioxygène au niveau de la mer est de 0,2 bar.
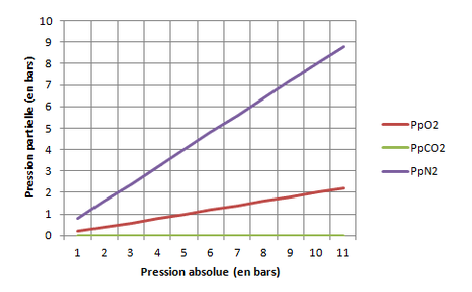
En répétant le calcul pour les 3 gaz et à profondeur variable on obtient les courbes ci-dessous (la variation de Pp CO2 n’apparait pas, elle varie seulement entre 0,0004 et 0,0044 bar).
En répétant le calcul pour les 3 gaz et à profondeur variable on obtient les courbes ci-dessous (la variation de Pp CO2 n’apparait pas, elle varie seulement entre 0,0004 et 0,0044 bar).
B) Le volume d’un gaz
Le corps humain, comme l’eau de mer, est incompressible c'est-à-dire que son volume sera très peu affecté par la pression environnante car il ne rétrécit pas en plongeant. En revanche tout gaz, comme ceux contenus dans l’air, sont eux, compressibles. Cette propriété particulière est énoncée par la loi de Boyle- Mariotte :
Le corps humain, comme l’eau de mer, est incompressible c'est-à-dire que son volume sera très peu affecté par la pression environnante car il ne rétrécit pas en plongeant. En revanche tout gaz, comme ceux contenus dans l’air, sont eux, compressibles. Cette propriété particulière est énoncée par la loi de Boyle- Mariotte :
P1 x V1 = P2 x V2
(à températures égales)
(à températures égales)
Cela revient à dire que, pour une même quantité de gaz de volume V1 à la pression atmosphérique P1 (par exemple celle contenue dans les poumons d’un plongeur en apnée), le volume V2 sera inférieur à V1 pour une pression supérieur à la pression atmosphérique. Donc, le volume d’air contenu dans les poumons d’un plongeur en apnée diminuera au fur et à mesure de sa descente (car la pression absolue qu’il subit augmentera) et inversement à la remontée.
Exemple : On considère un plongeur en apnée de volume pulmonaire 1 L (V1) à pression atmosphérique. On calcule alors son volume pulmonaire à une profondeur de 10 m :
-On pose Patm = P1 et Pabs = P2 (Pabs est la pression absolue subie par le corps du plongeur à 10 m de profondeur).
-On sait que P1 = 1 bar ; P2 = 2 bar
On a donc V2 = (P1 x V1) / P2 = 1 / 2 = 0.5 L
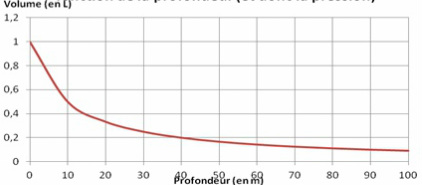
Le volume d’air contenu dans les poumons du plongeur en apnée à une profondeur de 10m est donc de 0.5 L. En renouvelant le calcul à différentes profondeurs, on obtient la courbe suivante.
Exemple : On considère un plongeur en apnée de volume pulmonaire 1 L (V1) à pression atmosphérique. On calcule alors son volume pulmonaire à une profondeur de 10 m :
-On pose Patm = P1 et Pabs = P2 (Pabs est la pression absolue subie par le corps du plongeur à 10 m de profondeur).
-On sait que P1 = 1 bar ; P2 = 2 bar
On a donc V2 = (P1 x V1) / P2 = 1 / 2 = 0.5 L
Le volume d’air contenu dans les poumons du plongeur en apnée à une profondeur de 10m est donc de 0.5 L. En renouvelant le calcul à différentes profondeurs, on obtient la courbe suivante.
Puisque la pression absolue du gaz à l’intérieur des poumons d’un plongeur est manipulée grâce au système de détendeur, afin d’être compensée par la pression imprimée par le milieu subaquatique, on déduit qu’un autre facteur intervient concernant le comportement des gaz en profondeurs.
C) Phénomène de dissolution.
Outre le phénomène de compressibilité des gaz, on assiste à un phénomène de dissolution. Un exemple courant démontrant cette propriété est l’eau gazeuse qui, à la pression atmosphérique (en opposition à la forte pression présente à l’intérieur de la bouteille fermée) émet une certaine quantité de bulles visibles à l’œil nu : le CO2 dissout à l’intérieur du liquide sous forme aqueuse est donc passé à l’état gazeux. Le corps humain étant composé à 70% d’eau, on peut supposer que ce phénomène s’applique également dans le cas de la plongée.
Ce phénomène est lié à la loi de Henry qui énonce : « À température constante et à saturation, la quantité de gaz dissous dans un liquide est proportionnelle à la pression partielle qu'exerce ce gaz sur le liquide. ». On a donc :
C) Phénomène de dissolution.
Outre le phénomène de compressibilité des gaz, on assiste à un phénomène de dissolution. Un exemple courant démontrant cette propriété est l’eau gazeuse qui, à la pression atmosphérique (en opposition à la forte pression présente à l’intérieur de la bouteille fermée) émet une certaine quantité de bulles visibles à l’œil nu : le CO2 dissout à l’intérieur du liquide sous forme aqueuse est donc passé à l’état gazeux. Le corps humain étant composé à 70% d’eau, on peut supposer que ce phénomène s’applique également dans le cas de la plongée.
Ce phénomène est lié à la loi de Henry qui énonce : « À température constante et à saturation, la quantité de gaz dissous dans un liquide est proportionnelle à la pression partielle qu'exerce ce gaz sur le liquide. ». On a donc :
Cs = Pp x H
-où Cs correspond à la concentration maximale dans le liquide, la saturation
-Pp correspond à la pression partielle de ce gaz appliqué à la surface du liquide
-H correspond à la constante de Henry qui dépend de la nature du gaz, de la température et de la nature du liquide. Son calcul est extrêmement compliqué.
-où Cs correspond à la concentration maximale dans le liquide, la saturation
-Pp correspond à la pression partielle de ce gaz appliqué à la surface du liquide
-H correspond à la constante de Henry qui dépend de la nature du gaz, de la température et de la nature du liquide. Son calcul est extrêmement compliqué.
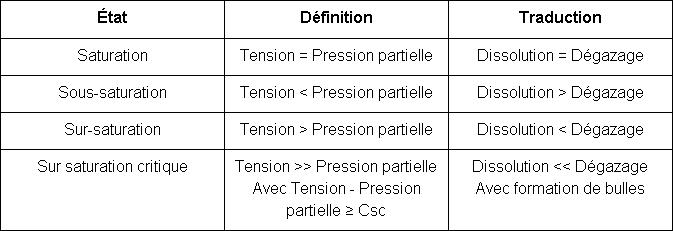
La « saturation » correspond au moment où la pression partielle d’un gaz et la pression qu’il exerce au sein du liquide (appelé tension) s’équilibrent. Cet état est atteint grâce à des échanges gazeux entre le mélange de gaz et le liquide : la dissolution et le dégazage. Lorsqu’un liquide et un gaz ont atteint la saturation, le liquide dissout alors autant de gaz qu’il en élimine.
Les liquides tendent naturellement vers la saturation quel que soit leur état initial. En effet, si un liquide est en sous-saturation, il absorbe du gaz en le dissolvant (car la tension est inférieure à la pression partielle du gaz), mais s’il est en sursaturation, il le restitue (car la tension est supérieure à la pression partielle du gaz). Ces deux états sont donc instables et se traduisent automatiquement par des échanges gazeux.
Il existe un quatrième état plus dangereux pour le plongeur que les trois précédents : la sursaturation critique. Il se définit par une différence trop importante entre la tension et la pression partielle d’un gaz se traduisant par un dégazage brutal sous forme de bulles. Le diamètre de ces bulles est proportionnel à la différence entre tension et pression partielle. On appelle coefficient de sursaturation critique (Csc) la différence entre la tension et la pression partielle à ne pas dépasser.
Les liquides tendent naturellement vers la saturation quel que soit leur état initial. En effet, si un liquide est en sous-saturation, il absorbe du gaz en le dissolvant (car la tension est inférieure à la pression partielle du gaz), mais s’il est en sursaturation, il le restitue (car la tension est supérieure à la pression partielle du gaz). Ces deux états sont donc instables et se traduisent automatiquement par des échanges gazeux.
Il existe un quatrième état plus dangereux pour le plongeur que les trois précédents : la sursaturation critique. Il se définit par une différence trop importante entre la tension et la pression partielle d’un gaz se traduisant par un dégazage brutal sous forme de bulles. Le diamètre de ces bulles est proportionnel à la différence entre tension et pression partielle. On appelle coefficient de sursaturation critique (Csc) la différence entre la tension et la pression partielle à ne pas dépasser.
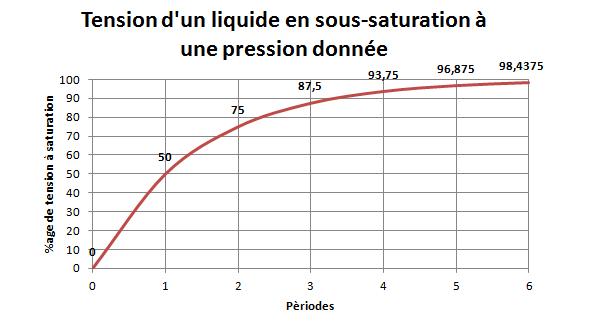
Toutefois, ces échanges gazeux ne se produisent pas instantanément ni de manière linéaire. En effet, on parle de période, ce qui correspond au temps nécessaire à un liquide pour dissoudre ou éliminer la moitié de la quantité nécessaire d’un gaz pour être en saturation. Sa durée varie selon la nature du liquide, la température ambiante (qui chez le plongeur, reste constamment à 37 °C) et l’agitation du liquide (la vitesse de circulation du sang qui augmente avec l’effort par exemple). De manière générale, on obtient la courbe suivante :
Par convention, on admet qu’après 6 périodes, la différence entre la tension d’un liquide et sa tension finale (tension à saturation) devient négligeable. On déduit de ce graphique que la quantité de gaz dissous à l’intérieur du sang du plongeur augmente avec la pression à laquelle il est exposé et la durée d’exposition. On peut donc supposer que ce phénomène influe sur la physiologie du plongeur.
Cette vidéo présente l'état du liquide (ici de l'eau gazeuse) lors d'une chute de pression sous cloche à vide. Pour illustrer cette progression, le ballon de baudruche situé en arrière plan augmente en volume, démontrant ainsi la loi de Boyle Mariotte.